La Ley de Boyle-Mariotte es una de las leyes fundamentales de la física que describe la relación entre la presión y el volumen de un gas a temperatura constante. Esta ley establece que, a temperatura constante, el volumen de un gas es inversamente proporcional a la presión que se ejerce sobre él. Fue formulada por Robert Boyle y Edme Mariotte en el siglo XVII.

Cómo se comprueba la ley de Boyle-Mariotte
La ley de Boyle-Mariotte se puede comprobar experimentalmente utilizando un dispositivo llamado manómetro. Este instrumento mide la presión de un gas en un recipiente cerrado y permite variar el volumen del mismo. Para comprobar la ley, se realiza una serie de mediciones de presión y volumen en diferentes condiciones y se verifica que su producto se mantiene constante.
Quién creó la ley de Boyle y Mariotte
La ley de Boyle-Mariotte fue formulada de manera independiente por Robert Boyle, un científico inglés, y Edme Mariotte, un científico francés. Boyle realizó sus experimentos en la década de 1660, mientras que Mariotte los llevó a cabo en la década de 1670. Ambos científicos llegaron a la misma conclusión de que la presión y el volumen de un gas están inversamente relacionados.
Cuáles son las variables de la ley de Boyle
La ley de Boyle-Mariotte se basa en dos variables principales: la presión y el volumen. Estas variables están inversamente relacionadas, lo que significa que si se aumenta la presión sobre un gas, su volumen disminuirá, y viceversa. Es importante destacar que esta ley solo se aplica a gases ideales a temperatura constante.
Además de la presión y el volumen, la ley de Boyle-Mariotte también implica la temperatura absoluta. Aunque esta ley considera la temperatura constante, tener en cuenta que la temperatura puede afectar la presión y el volumen de un gas en otras circunstancias.

La ecuación de la ley de Boyle-Mariotte
Matemáticamente, la ley de Boyle-Mariotte se puede expresar mediante la siguiente ecuación:

P * V = constante
Donde:
- P es la presión del gas
- V es el volumen del gas
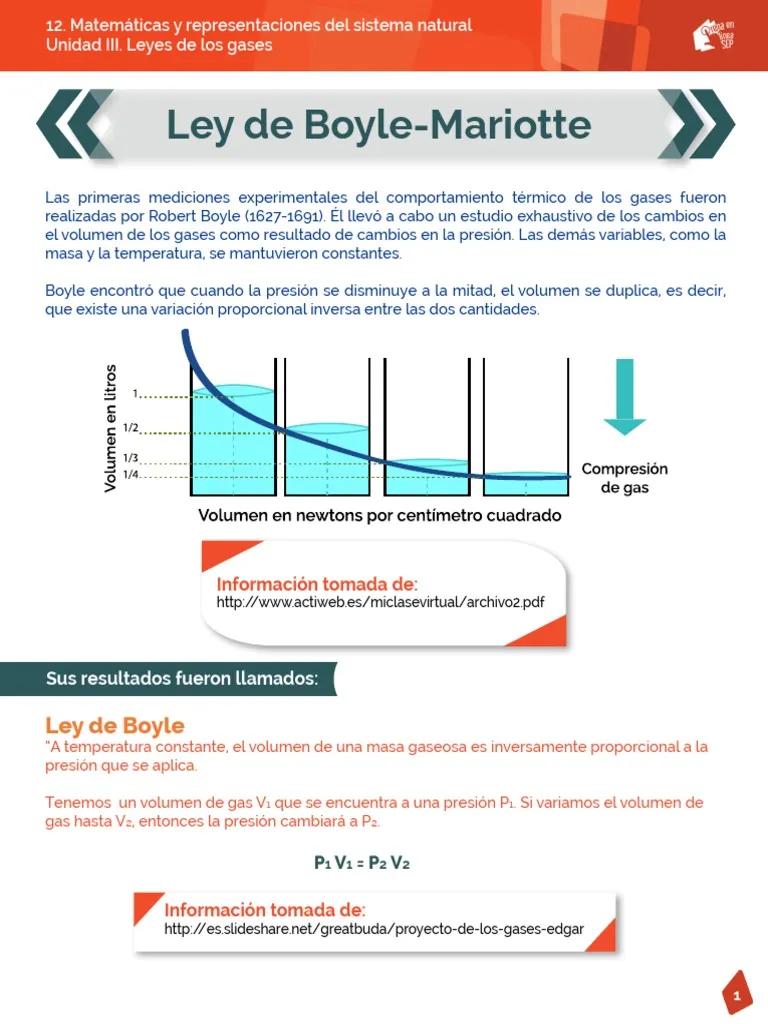
Esta ecuación muestra que el producto de la presión y el volumen de un gas se mantiene constante a temperatura constante. Esto significa que si se duplica la presión sobre un gas, su volumen se reducirá a la mitad, y viceversa.
Aplicaciones de la ley de Boyle-Mariotte
La ley de Boyle-Mariotte tiene numerosas aplicaciones en la vida cotidiana y en la ciencia. Algunas de estas aplicaciones incluyen:
- Funcionamiento de los sistemas de aire acondicionado y refrigeración
- Funcionamiento de los compresores de aire
- Funcionamiento de los motores de combustión interna
- Estudio de la respiración y la ventilación pulmonar
- Estudio de los procesos de compresión y expansión de gases
La ley de Boyle-Mariotte establece que la presión y el volumen de un gas están inversamente relacionados a temperatura constante. Esta ley es fundamental en la comprensión de los gases y tiene diversas aplicaciones en la vida cotidiana y en la ciencia.

